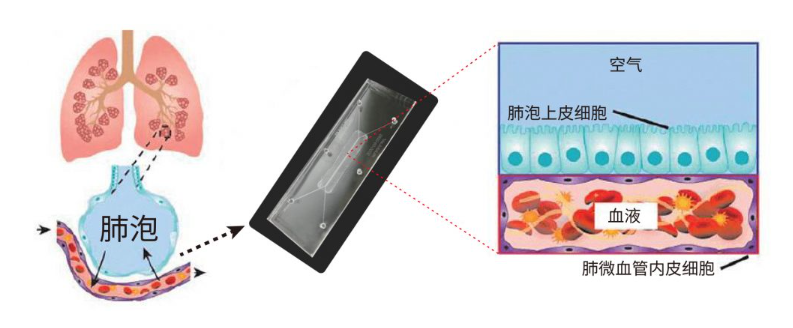
細(xì)胞培養(yǎng)開始于 19 世紀(jì)末���,在過去一個(gè)世紀(jì)中��,維持和分析貼壁細(xì)胞系最流行的方法是 2D 或單層培養(yǎng),但科學(xué)家們一直試圖解決一個(gè)問題��,如何讓細(xì)胞在體外活的更真實(shí)呢�?2D細(xì)胞培養(yǎng)像是“細(xì)胞住平板房”(圖1)�,但真實(shí)的人體是“細(xì)胞住立體社區(qū)”(圖2) ����,而細(xì)胞3D培養(yǎng)是一種將細(xì)胞在三維空間進(jìn)行培養(yǎng)的技術(shù),能更好的在體外模擬體內(nèi)環(huán)境��,彌補(bǔ)了傳統(tǒng)2D細(xì)胞培養(yǎng)的不足�����。
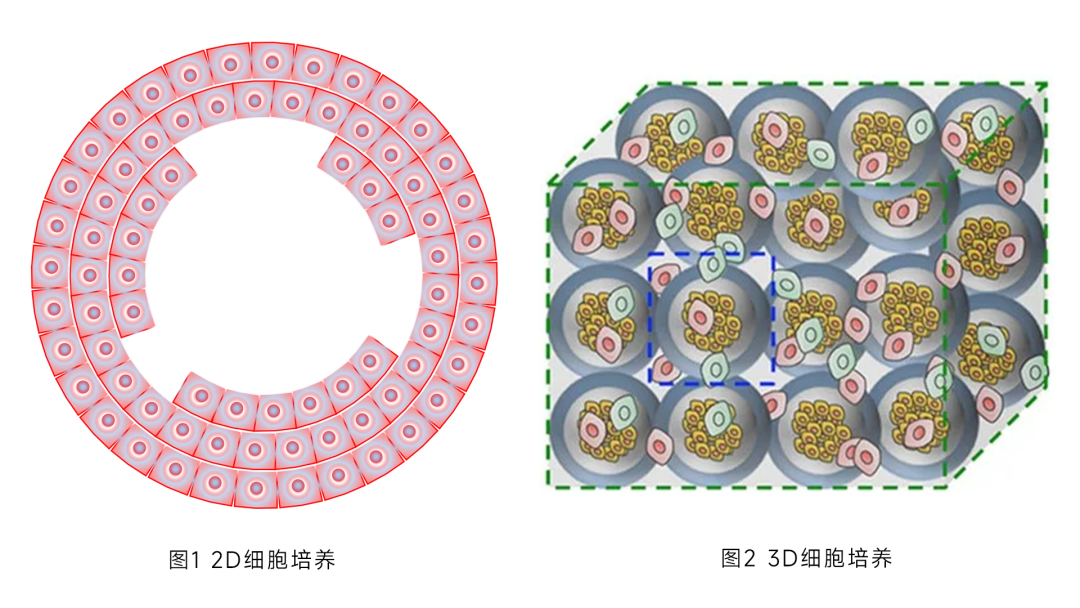
2D培養(yǎng)中細(xì)胞對培養(yǎng)基中營養(yǎng)物質(zhì)和生長因子的攝取方式與體內(nèi)不同,所有細(xì)胞接收到的營養(yǎng)和因子基本相同�,缺乏體內(nèi)復(fù)雜的化學(xué)梯度����。細(xì)胞與細(xì)胞外基質(zhì)(ECM) 的相互作用也被簡化,無法體現(xiàn)體內(nèi)細(xì)胞與 ECM 離散連接的特點(diǎn)�,影響細(xì)胞的信號傳導(dǎo)���、增殖和分化等過程。
由于上述原因���,2D 培養(yǎng)在藥物敏感性�����、細(xì)胞增殖速率���、基因和蛋白質(zhì)表達(dá)水平等方面與體內(nèi)模型存在顯著差異。在藥物測試中����,2D 培養(yǎng)的細(xì)胞往往對藥物更敏感,導(dǎo)致對藥物療效的評估不準(zhǔn)確,難以反映藥物在體內(nèi)的真實(shí)效果�,增加了藥物研發(fā)的風(fēng)險(xiǎn)和成本����。
模擬體內(nèi)真實(shí)環(huán)境
體內(nèi)細(xì)胞處于復(fù)雜的三維環(huán)境中,與周圍細(xì)胞和 ECM 緊密相互作用�。3D 培養(yǎng)能夠更好地模擬這種環(huán)境����,使細(xì)胞呈現(xiàn)自然的形態(tài)和極性��,有利于細(xì)胞間的信號傳導(dǎo)和物質(zhì)交換�����,更準(zhǔn)確地反映細(xì)胞在體內(nèi)的行為和功能,如細(xì)胞的增殖����、分化、遷移等過程�����。
提高實(shí)驗(yàn)準(zhǔn)確性
在藥物研發(fā)、疾病研究等領(lǐng)域���,3D 培養(yǎng)的細(xì)胞對藥物的反應(yīng)更接近體內(nèi)情況�,能夠提供更可靠的實(shí)驗(yàn)數(shù)據(jù)�。通過 3D 培養(yǎng)可以更準(zhǔn)確地評估藥物的療效和毒性��,減少動物實(shí)驗(yàn)的需求�,提高研究效率和成功率。
深入研究細(xì)胞行為和疾病機(jī)制
3D 培養(yǎng)有助于研究細(xì)胞在復(fù)雜環(huán)境中的行為����,如腫瘤細(xì)胞的侵襲和轉(zhuǎn)移��、干細(xì)胞的分化調(diào)控等���。對于理解疾病的發(fā)生����、發(fā)展機(jī)制���,以及開發(fā)新的治療方法具有重要意義����。
微流控概念
微流控是一種操控微小體積流體的技術(shù)��,它能夠在微觀尺度上精確控制流體的流動��、混合���、分配等行為�����。通過在芯片上構(gòu)建微小的通道、閥門���、反應(yīng)室等結(jié)構(gòu),實(shí)現(xiàn)對生物�、化學(xué)等過程的精確控制和分析。
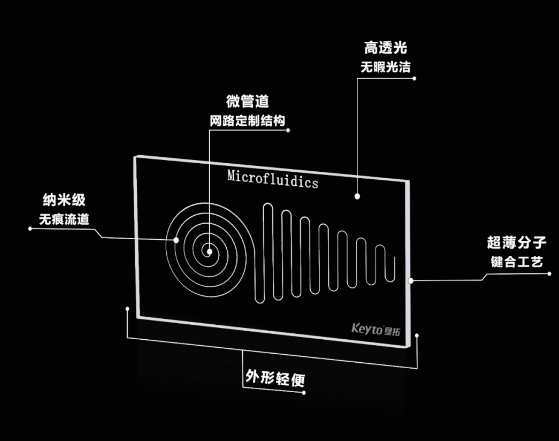
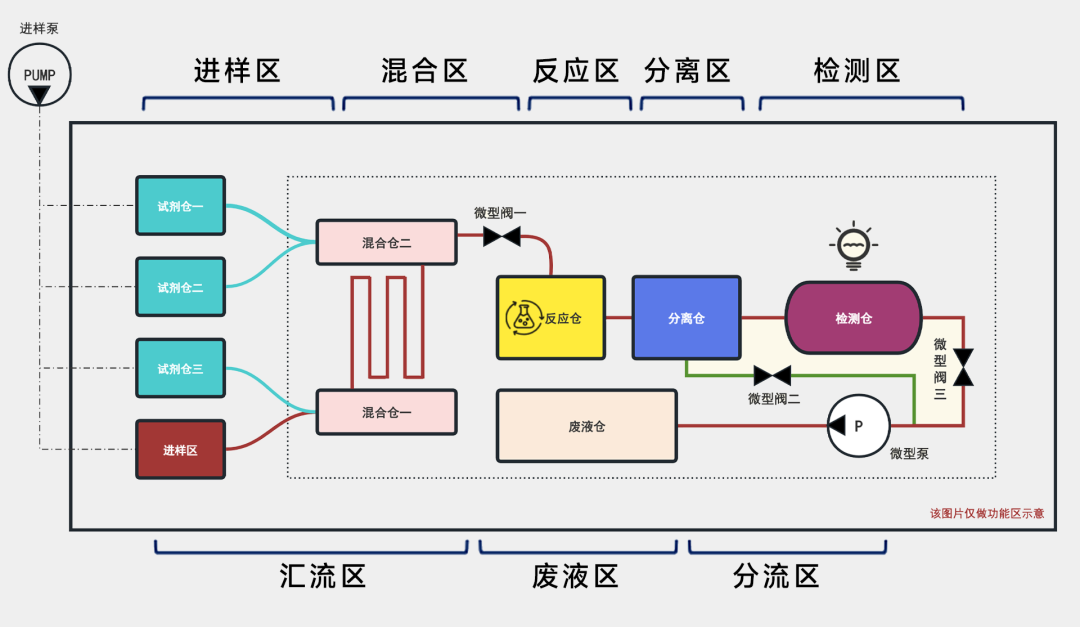
微流控技術(shù)具有體積小、消耗低��、通量高���、可集成化等優(yōu)點(diǎn)�,在生物醫(yī)學(xué)����、化學(xué)分析等領(lǐng)域有廣泛應(yīng)用�����。在細(xì)胞培養(yǎng)方面���,微流控系統(tǒng)可以為細(xì)胞提供更接近體內(nèi)的微環(huán)境�,實(shí)現(xiàn)對細(xì)胞生長���、分化���、相互作用等過程的精確調(diào)控和監(jiān)測����。
精確控制微環(huán)境
微流控系統(tǒng)可以精確調(diào)控細(xì)胞培養(yǎng)的微環(huán)境����,如通過控制流體流動來調(diào)節(jié)營養(yǎng)物質(zhì)��、生長因子的濃度和分布,模擬體內(nèi)的化學(xué)梯度�����。還能調(diào)節(jié)微環(huán)境的物理參數(shù)���,如剪切應(yīng)力�、基質(zhì)剛度等�,為 3D 培養(yǎng)的細(xì)胞提供更接近體內(nèi)的生長條件��。
實(shí)現(xiàn)高通量和自動化
微流控技術(shù)適合高通量實(shí)驗(yàn)����,能夠同時(shí)培養(yǎng)多個(gè)樣本�,提高實(shí)驗(yàn)效率。結(jié)合自動化設(shè)備(圖3)�,可以實(shí)現(xiàn)細(xì)胞接種�����、培養(yǎng)基更換���、數(shù)據(jù)采集等過程的自動化,減少人為誤差��,提高實(shí)驗(yàn)的可重復(fù)性和可靠性�����。
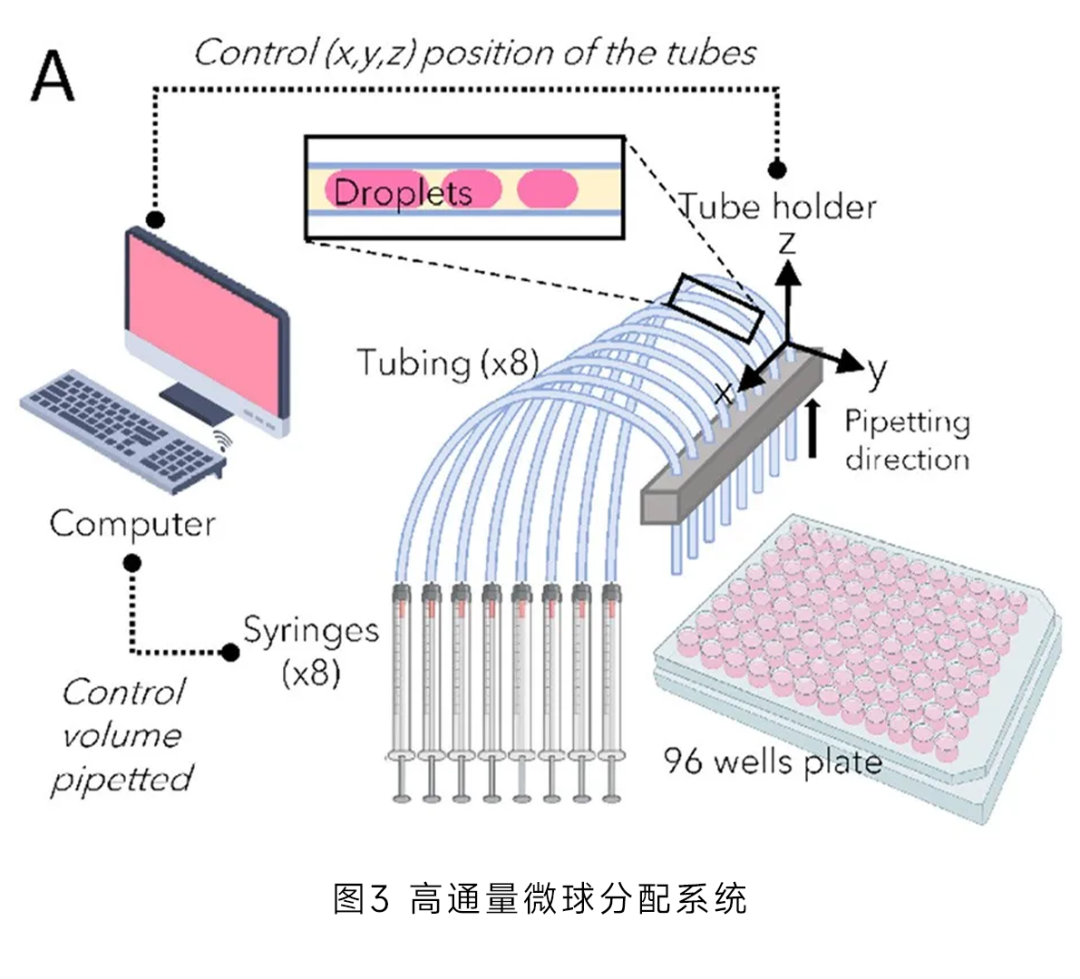
便于集成檢測和分析
微流控芯片可以集成多種檢測和分析功能(圖4)���,如光學(xué)檢測、電化學(xué)檢測等��,能夠?qū)崟r(shí)�、原位地監(jiān)測細(xì)胞的生長狀態(tài)�、代謝活動���、基因表達(dá)等指標(biāo)�����,為 3D 細(xì)胞培養(yǎng)提供豐富的信息,有助于深入了解細(xì)胞的行為和功能���。

04
微流控在細(xì)胞3D培養(yǎng)中的案例
微球封裝細(xì)胞
基于微流控芯片內(nèi)部的微通道網(wǎng)絡(luò)�����,利用流體力學(xué)原理�����,將含有細(xì)胞的生物溶液與用于形成微球的材料溶液(如聚合物溶液��、水凝膠)在微通道中精確操控和混合��。通過調(diào)節(jié)微通道的尺寸�、流體流速等參數(shù)���,使兩種溶液在特定位置形成微小的液滴或微球結(jié)構(gòu),細(xì)胞被包裹在這些微球內(nèi)部�,隨后經(jīng)過物理或化學(xué)方法使微球固化成型,從而實(shí)現(xiàn)細(xì)胞的穩(wěn)定包裹 (圖5)�����。
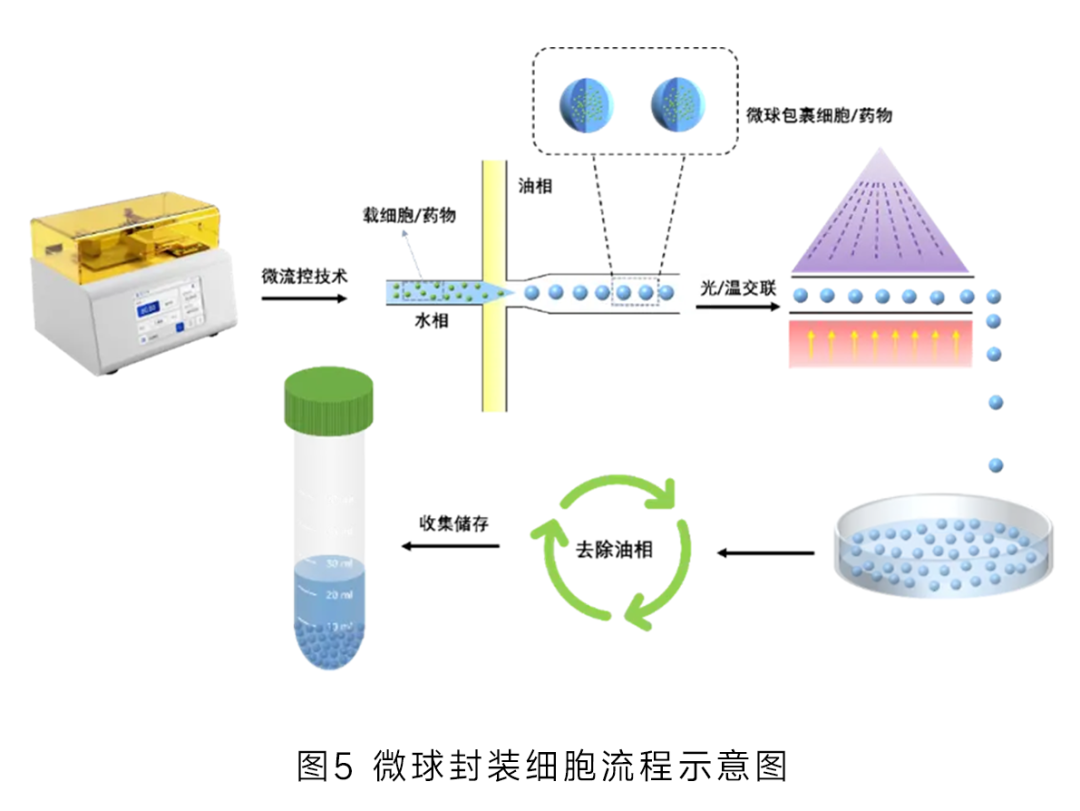
疾病模型構(gòu)建
在腫瘤研究領(lǐng)域,深入探究腫瘤侵蝕血管的機(jī)制至關(guān)重要���,它對于理解腫瘤轉(zhuǎn)移和開發(fā)有效的抗癌療法意義重大��。
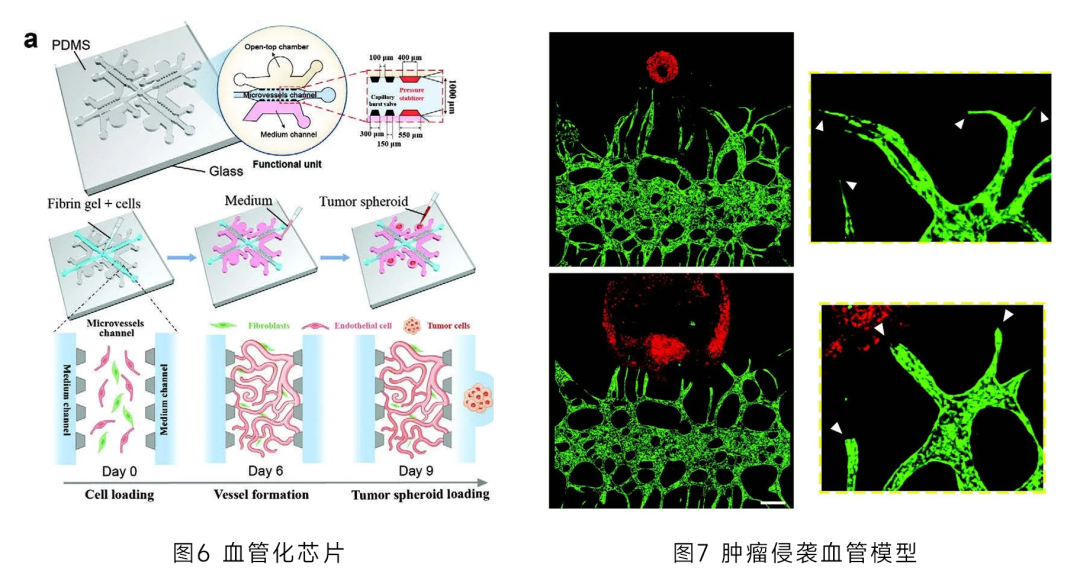
微流控技術(shù)作為一種前沿技術(shù)���,能夠在微小的通道內(nèi)精確操控流體,為模擬生物體內(nèi)微環(huán)境提供了有力手段�����;而血管化芯片則可構(gòu)建出具有血管結(jié)構(gòu)的微環(huán)境(圖6)����。將兩者結(jié)合用于研究腫瘤侵蝕血管時(shí)���,首先在微流控芯片上精心構(gòu)建出包含血管結(jié)構(gòu)的三維微環(huán)境,通過精確控制流體����,模擬體內(nèi)血液循環(huán)�����。接著將腫瘤細(xì)胞引入該微環(huán)境中�,觀察腫瘤細(xì)胞在血管化芯片上的生長����、遷移以及與血管相互作用的過程(圖7)。
研究人員能夠?qū)崟r(shí)監(jiān)測腫瘤細(xì)胞如何突破血管壁�����、侵入血管內(nèi)部�,分析其侵蝕血管的分子機(jī)制和影響因素���。這一研究方法不僅克服了傳統(tǒng)研究模型的局限性,還能在微觀層面為腫瘤侵蝕血管的研究提供更精準(zhǔn)�����、更詳細(xì)的數(shù)據(jù)���,有助于推動腫瘤治療領(lǐng)域的新突破。
器官模型構(gòu)建
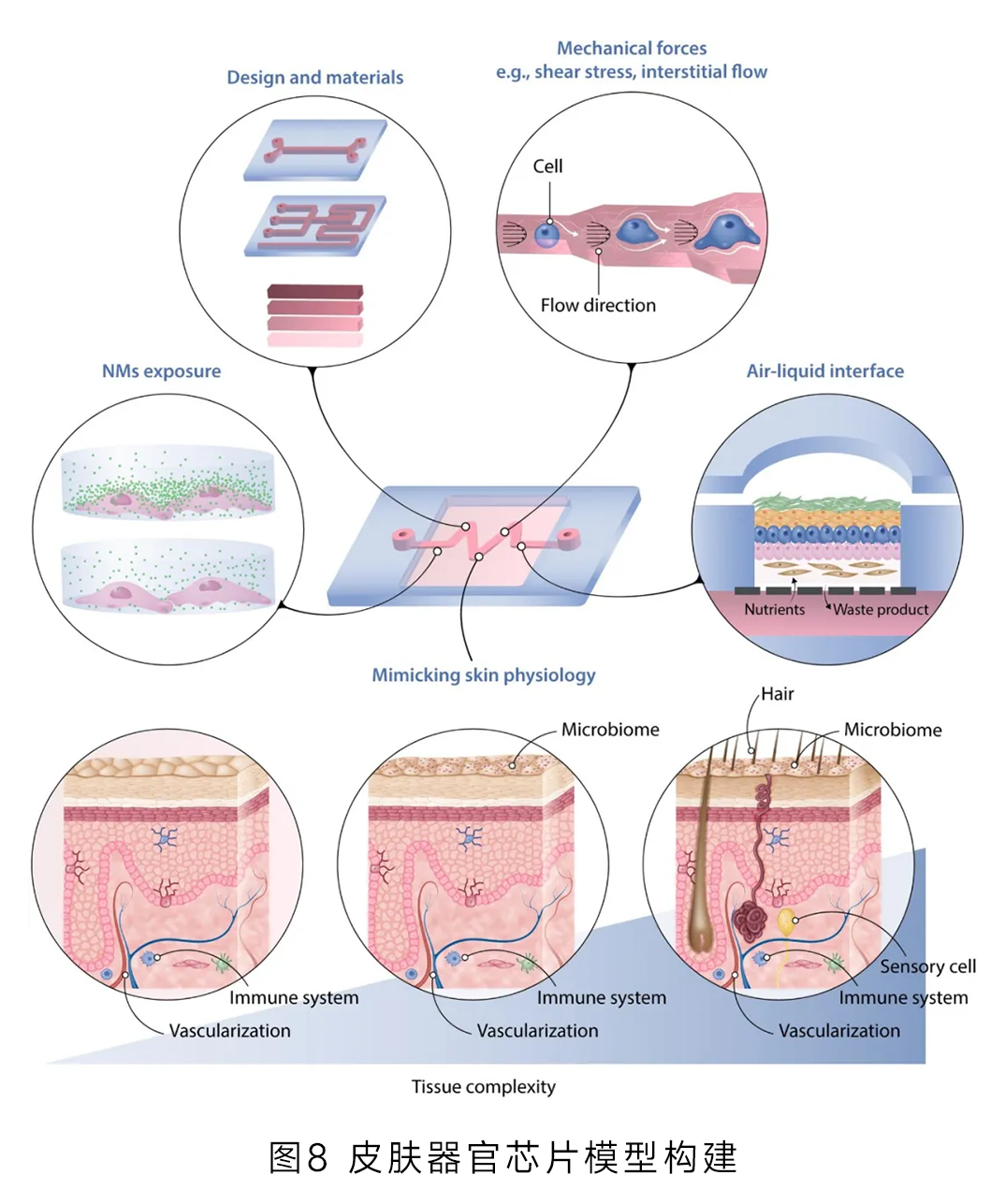
微流控技術(shù)能在微小通道內(nèi)精確操控流體�,皮膚器官芯片則模擬了人體皮膚的結(jié)構(gòu)和功能,二者結(jié)合為皮膚研究帶來了革新���。歐萊雅已成功運(yùn)用這一技術(shù)組合�����,用皮膚芯片替代動物測試。
在這一應(yīng)用中����,微流控技術(shù)精準(zhǔn)控制營養(yǎng)物質(zhì)����、藥物等流體在皮膚器官芯片中的輸送,模擬皮膚在不同環(huán)境下的生理狀態(tài)�。
皮膚器官芯片由多種細(xì)胞和細(xì)胞外基質(zhì)構(gòu)建�����,高度還原真實(shí)皮膚組織(圖8)���;這一替代不僅避免了動物實(shí)驗(yàn)倫理爭議�,還提供了更精準(zhǔn)、更具生理相關(guān)性的測試結(jié)果���,以更科學(xué)�、更人道的方式評估產(chǎn)品功效與安全性,推動行業(yè)朝著綠色�、可持續(xù)方向發(fā)展�。
05
在生命科學(xué)快速發(fā)展的時(shí)代�����,微流控與細(xì)胞3D培養(yǎng)的結(jié)合展現(xiàn)出極為廣闊的前景����。未來,隨著技術(shù)的不斷創(chuàng)新�����,二者融合有望在醫(yī)學(xué)領(lǐng)域?qū)崿F(xiàn)重大突破,例如構(gòu)建高度仿真的人體器官模型,助力疾病機(jī)制的深入研究���,為個(gè)性化醫(yī)療方案的制定提供精準(zhǔn)依據(jù)��。
在制藥行業(yè)����,能夠更高效地篩選和評估藥物,極大縮短新藥研發(fā)周期��,降低研發(fā)成本����。在組織工程方面,可制造出具有復(fù)雜結(jié)構(gòu)和功能的人造組織與器官���,緩解器官移植供體短缺的困境。
此外���,隨著微流控技術(shù)在微尺度操控上的進(jìn)一步優(yōu)化,細(xì)胞3D培養(yǎng)體系的不斷完善�,二者的結(jié)合將在生物傳感器開發(fā)����、再生醫(yī)學(xué)等新興領(lǐng)域持續(xù)拓展�,為解決人類健康問題帶來更多可能����,推動整個(gè)生命科學(xué)領(lǐng)域邁向新的高度�����。
Jensen C, Teng Y. Is it time to start transitioning from 2D to 3D cell culture?[J]. Frontiers in molecular biosciences, 2020, 7: 33.
[2] Ko J, Park D, Lee J, et al. Microfluidic high-throughput 3D cell culture[J]. Nature Reviews Bioengineering, 2024, 2(6): 453-469.
[3] Castiaux A D, Spence D M, Martin R S. Review of 3D cell culture with analysis in microfluidic systems[J]. Analytical Methods, 2019, 11(33): 4220-4232.
素材來源:官方媒體/網(wǎng)絡(luò)資訊








 language
language